Was sind klinische Studien?
Klinische Studien sind wissenschaftliche, genau geplante Untersuchungen, mit denen
- neue medizinische Behandlungen,
- Medikamente,
- Wirkstoffe oder
- Diagnoseverfahren
systematisch geprüft werden.
Ziel ist es, deren Wirksamkeit, Sicherheit und mögliche Nebenwirkungen unter kontrollierten Bedingungen zu untersuchen. Dabei folgen klinische Studien strengen ethischen und gesetzlichen Vorgaben, um den Schutz der Teilnehmenden zu gewährleisten.
In der Regel werden sie in mehrere Phasen unterteilt: von ersten Tests zur Verträglichkeit bis hin zu großen Studien, die zeigen sollen, ob eine neue Therapie besser oder gleichwertig zu bestehenden Methoden ist. Für Patientinnen und Patienten bieten klinische Studien die Möglichkeit, frühzeitig Zugang zu innovativen Behandlungen zu erhalten, während sie gleichzeitig einen wichtigen Beitrag zum medizinischen Fortschritt leisten.
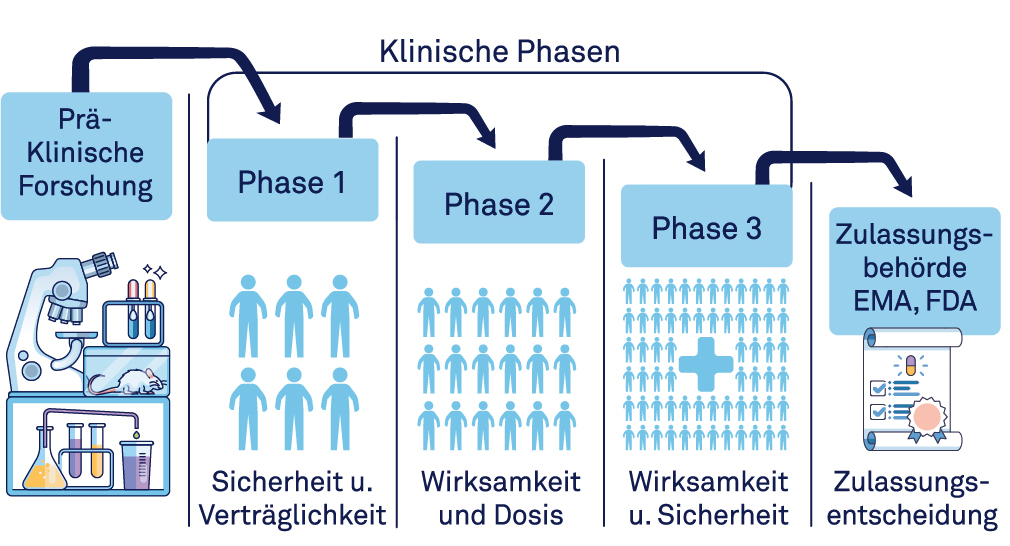
Klinische Phasen
Phase 1: Diese erfasst das Sicherheits- und Verträglichkeitsprofil eines Medikaments, bestimmt eine mögliche Dosis und untersucht, wie sich das Medikament im Körper verteilt und wieder ausgeschieden wird (Pharmakokinetik).
Phase 2: Diese prüft, ob die Medikation bei einer (größeren) Gruppe an Patient:innen mit einer bestimmten Erkrankung wirksam ist und stellt die geeignete Dosis fest.
Phase 3: Diese prüft die Wirksamkeit und Sicherheit gewöhnlich bei mehreren hundert bis tausenden Patient:innen meist im Vergleich zu verfügbaren Behandlungen und führt im Idealfall zur Zulassung des Medikaments.
Studienteilnahme
Haben Sie Interesse an einer Studie teilzunehmen?
Unter nachfolgendem Link kommen Sie zum Anmeldeformular - hier können Sie sich unverbindlich registrieren und wir melden uns, wenn eine Studie zu Ihnen passt. Wir suchen häufig auch gesunde Freiwillige, die sich ebenfalls über dieses Formular registrieren können.
Alternativ können sie unsere Studien, für die aktiv Proband:innen gesucht werden, hier einsehen.
